一、病毒的生活周期与抗病毒药物靶标
病毒是严格的细胞内寄生的微生物,在细胞外病毒不能存活和增殖。动物病毒与植物病毒以及细菌病毒(噬菌体)的生活周期有较大的区别。抗病毒药物研究主要关注的是动物病毒,特别是人类病毒。所有动物病毒的生活周期大致上分为以下几个阶段:
1.吸附进入:病毒通过其包膜(有包膜病毒)或衣壳(无包膜病毒)上的结构蛋白与宿主细胞膜上的受体(和/或共受体)结合,从而介导病毒的吸附和进入(各种方式的内吞)。
2. 病毒核酸的复制和转录:通常在膜融合后,病毒的核酸(一般与核蛋白形成复合物)进入到复制地点,多数DNA病毒和少数的RNA病毒在细胞核内复制和转录,少数DNA病毒(如痘苗病毒)和多数RNA病毒(如HCV)在细胞质内复制和转录。根据病毒核酸类型的不同,复制和转录的详细机制大不相同,但都需要有病毒编码的聚合酶参与,同时也需要大量的宿主因子参与,有时候宿主的聚合酶也会参与病毒复制或转录的步骤。
3. 病毒蛋白的翻译和转运:病毒蛋白的翻译和运输完全依赖于宿主细胞的翻译机器和运输系统,翻译后的病毒蛋白会被运送到细胞核或细胞质的特定位置,与病毒核酸及其它结构蛋白分步骤组装成病毒的核衣壳。
4. 病毒的出芽和释放:有包膜病毒通常以出芽的方式获得包膜和释放到胞外,而无包膜病毒可以通过细胞裂解的方式释放到胞外。
病毒生活周期看似复杂,每一步都有多种蛋白分子参与,但是病毒的生活周期(复制)是单线条的,只要抑制了该链条上的任意一个(病毒的或者宿主的)蛋白的功能,从而影响了病毒复制的一个小的步骤,就能达到抑制病毒复制的目的。抗病毒药物研发中应该充分了解相关病毒的生活周期,并在此基础上谨慎选择药物靶标,从而实现药物的有效抗病毒作用和适当的广谱性,并尽可能减少药物对宿主的毒性作用。现有的抗病毒药物根据其靶标的不同,可以分成两大类:即作用于宿主靶标的抗病毒药物HTAs和直接作用于病毒靶标的抗病毒药物DAAs。从理论上上讲,DAA类抗病毒药物毒性可能会小一些(如果脱靶效应低),但是容易产生耐药的病毒株。而HTA类药物,因作用于宿主靶标,可能会产生较大的毒性,但是不大可能产生耐药性突变病毒株。对某个具体的病毒感染而言,如何选择靶标应该从病毒的亚型、生活周期、病毒感染的靶器官/组织、病程和致病特点等多方面的因素综合考量。无论选择的是哪种靶标,研发出的新药的药效及安全性必须在体外和体内进行严谨的验证。
二、基于靶标的体外抗病毒药物筛选技术
基于靶标的体外筛选,是指在人为设定的反应条件下筛选可与一个孤立的靶标相互作用的化合物。病毒的基因组一般很小,仅能编码不多的几个蛋白,通常包括结构蛋白、聚合酶和复制相关的蛋白等。在一些情况下可以考虑从基于靶标的体外筛选开始抗病毒药物的研究。比如,对于某些烈性病毒开展活病毒的研究需要在P3或者P4实验室中进行,可以先针对病毒的重要蛋白开展抑制剂的研究;对于病毒编码的具有酶活性的靶标分子(如聚合酶、蛋白酶、神经氨酸酶等),可以建立基于靶标活性的体外生物化学反应的筛选模型筛选抑制剂;对于存在(蛋白)分子相互作用的靶标,可以通过体外分子相互作用检测仪实现筛选;对于结构已经解析的靶标分子,还可以通过计算机进行虚拟(in silicon)筛选。基于靶标的体外筛选技术经常采用各种基于荧光和化学发光,以及荧光共振能量转移等技术,让筛选变得简便。基于靶标的体外筛选技术也可以用于验证通过其它方法得到的特定靶标的抑制剂是否能抑制该靶标。
基于靶标的体外筛选中,由于靶标分子(通常是蛋白质)需要通过某些体系表达和纯化,或者从病毒感染的细胞裂解液中纯化,体外反应与真实的体内病毒复制过程中的反应可能有较大差异。所以,基于靶标的体外筛选技术不应该作为首选。通过基于靶标的体外筛选得到的阳性化合物(hits),假阳性会比较多。其抗病毒活性必须通过活病毒细胞感染实验进行验证。
三、基于细胞的抗病毒药物筛选技术
基于细胞的筛选技术是抗病毒药物研究中最常用的技术,也是最重要的技术之一。因为病毒要从感染细胞开始,在允许细胞中完成复制,产生并释放出具有感染性的病毒颗粒,才能完成其生活周期。病毒对感染的细胞有非常严格的要求,以实现其复制的目的。一个具体的病毒感染人或动物时,通常只能感染少数的组织和器官,或者只能感染一种组织器官(如肝脏)。因此开展基于细胞的筛选,首先是准备合适的能支持病毒复制且尽可能与疾病相关的细胞株。其次是病毒株的选择,尽可能选择临床分离株或实验株的病毒。经过改造的报告病毒虽然会给筛选带来方便,但也可能出现筛选到的抑制剂对临床分离株病毒无效的情况。根据具体的病毒种类,有时候可能需要选用一种以上的细胞株或者病毒株。
基于细胞的筛选技术大致上可以分为以下4种筛选技术。
(一)表型的终点检测
病毒感染细胞后在细胞内复制,通常会产生特定的表型。最常见的表型包括细胞裂解、产生细胞病变、形成合胞体等。常用于检测病毒复制水平的终点有空斑数量以及细胞病变效应(cytopathic effect,CPE),并由此而产生出两种实验用于检测药物在细胞水平对病毒复制的抑制作用,即空斑减少实验和细胞病变减少实验。空斑减少实验中,空斑的数量近似等于感染性病毒的数量,少数空斑可能由1个以上的病毒感染产生。所以如果能观察到浓度依赖的空斑减少效应,则表明药物有抗病毒作用(图1)。细胞病变减少实验中,对于能产生明显细胞病变或细胞裂解的病毒,其引起细胞病变的程度与病毒的复制水平呈正比。所以如果能观察到浓度依赖的细胞病变减少,则表明药物有抗病毒作用(图2)。以上两种基于表型的终点检测实验,空斑减少实验的定量更为准确,但相对难于操作;而细胞病变减少实验易于操作,可以选择使用各种细胞存活率检测试剂盒来检测终点。但有时候读值(read-out)与病毒复制水平的线性关系不好。因此在使用前要检测方法的有效性。
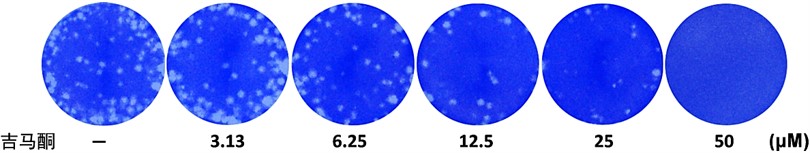
图1.吉马酮在空斑减少实验中能浓度依赖性地抑制流感病毒PR8株在MDCK细胞中的复制。
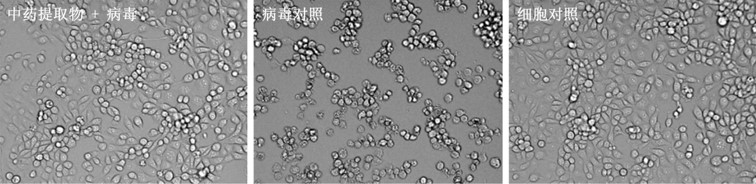
图2. 具有抗人副流感病毒作用的中药提取物能通过抑制病毒复制减少人副流感病毒HPIV3株在LLC-MK2细胞引起的细胞病变效应。
(二)基于细胞的单靶标检测
对于不能产生裂解性复制且不产生细胞病变的病毒,可以检测病毒编码的蛋白或病毒核酸的水平来反映药物对病毒复制水平的影响。由于不同的化合物可能会抑制病毒复制周期的不同阶段,药物对不同的病毒靶标分子的影响也是不同的,因此应该谨慎选择所检测的靶标分子,必要时可以检测多个靶标分子。常用的单靶标检测方法主要有病毒抗原减少实验和病毒基因组拷贝数减少实验(图3A,B)。单靶标的检测有时不能准确反映药物的抗病毒作用,抗病毒药效检测的金标准是药物对感染性病毒颗粒产生的影响(通过空斑减少实验或滴度减少实验检测)(图3C)。
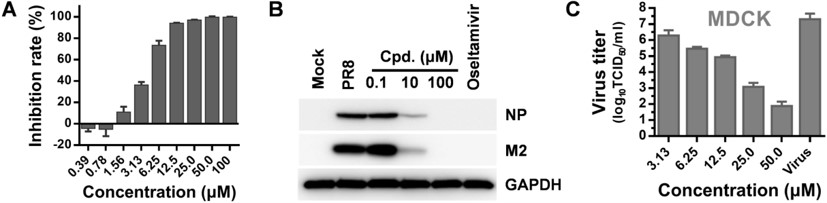
图3.候选药物对流感病毒的抑制作用。 A.药物减少流感病毒NA的水平;B. 药物减少流感病毒NP及M2的水平;C. 药物对感染性病毒颗粒产生的影响(滴度减少实验)。
(三)报告基因检测
在抗病毒药物研究中,为了便于高通量筛选,研究者有时会通过改造病毒或者细胞,构建含有报告基因(如绿色荧光蛋白或荧光素酶)的病毒(被称为报告病毒),或者含报告基因的细胞。报告病毒如果能构建成功,病毒的复制水平(影响绿色荧光蛋白或荧光素酶表达水平)可以很容易地被看到或者定量,大大方便了高通量抗病毒药物筛选。但是在实际应用中的问题主要有二,一是报告基因很容易随病毒发生某些突变而失去报告的功能,但不影响病毒复制水平;二是报告病毒可能在某些方面与野生型病毒株有所不同,对药物的反应也可能有所不同。报告细胞则是含有能被特定的病毒蛋白调控表达的报告基因的细胞系,通常难以构建成功。此外,由于RNA病毒容易变异,报告基因会随着病毒传代而发生变异,最终失去报告基因的功能。解决的方法是减少报告病毒的传代,或只用初代。图4中HCV GFP报告病毒能反映药物利巴韦林对病毒复制的抑制作用。

图4. HCV报告病毒在抗病毒药物筛选中的应用。左图显示利巴韦林浓度依赖地减少HCV报告病毒GFP的表达水平,右图显示利巴韦林浓度依赖地减少HCV NS3蛋白的水平。


